米国における医薬品および医療機器の規制当局にあたる米食品医薬品局(FDA)はこのほど、ポイントオブケアのための「3Dプリント医療機器」について、その規制に焦点を当てた新しいディスカッションペーパーを公表した。
同局のCenter for Devices and Radiological Health(CDRH)は当該文書を公開し、「医療機器業界、メーカー、医療従事者、医療機関、その他の関係者」からの意見を広く求めている。ディスカッションペーパーには、3Dプリント技術の簡単な歴史と、3Dプリント設備が機器の安全性・有効性にどのような影響を与えるかについて、現時点でのFDAの見解が記載されている。また、病院・クリニック・その他医療施設での機器のプリントに関連し、いくつかの重要な課題についても詳しく解説を加えている。
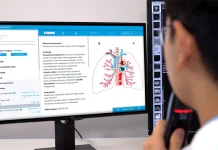
CDRHの機器評価部門でディレクターを務めるWilliam Maisel医師は「医療機器の3Dプリントは、イノベーションとヘルスケアの最前線にある」と述べ、技術の活用が今後さらに広がることに触れる。その上で、「患者に個別最適化した装置や手術計画用の解剖学的モデルを迅速に作成できる」といった医療者向けとしての、従前の利用用途拡大だけではなく、「医療施設が患者ニーズに迅速に対応するのに役立つ多くの用途がある」と、その利用領域の広さに言及している。
18ページに及ぶ「3D Printing Medical Devices at the Point of Care」は、FDAのウェブサイトから入手・閲覧が可能となっているので、ぜひ参照のこと。
関連記事: